영남대, 전자현미경 이용 ‘초소형 단백질 구조’ 규명
||2026.05.06
||2026.05.06
영남대학교(총장 최외출)는 김동영 약학부 교수 연구팀이 이론적으로 초저온전자현미경(Cryo-EM)으로는 분석이 어렵다고 알려졌던 초소형 단백질의 구조를 세계 최초로 규명했다고 6일 밝혔다.
단백질은 우리 몸에서 다양한 기능을 수행하는 핵심 물질이다. 단백질 구조는 기능을 결정하는 중요한 정보다. 단백질 구조를 정확히 파악하는 연구는 질병 원인 규명과 신약 개발의 기초가 된다.
그동안 단백질 구조 분석에는 강력한 X-선을 이용하는 'X-선 결정학'이 널리 활용 되어왔다. X-선 결정학은 단백질을 결정 형태로 만든 뒤 X-선을 쏘아 구조를 계산하는 방식이지만, 단백질을 결정화하는 과정에서 실험적 제약이 크고, 많은 시간과 노력이 필요하다는 한계가 있다.
이러한 문제를 극복하기 위해 시료의 이미지를 수집하여 구조를 분석하는 초저온전자현미경 기술이 주목받고 있으며, 최근 해상도 혁신을 통해 단백질 입체구조 분석의 핵심 기법으로 자리잡고 있다.
다만 초저온전자현미경은 일반적으로 200kDa(단백질의 크기를 나타내는 단위) 이상의 큰 단백질 분석에는 효과적이지만, 작은 단백질의 경우 구조분석에 한계가 있는 것으로 알려져 왔다. 2017년 노벨화학상 수상자인 리처드 헨더슨이 제시한 이론에 따르면 전자현미경으로 분석 가능한 단백질의 최소 크기는 약 38kDa이며, 실제로 지금까지 보고된 가장 작은 크기의 전자현미경 구조도 46kDa 수준으로, 38kDa는 사실상 한계 크기로 여겨져 왔다.
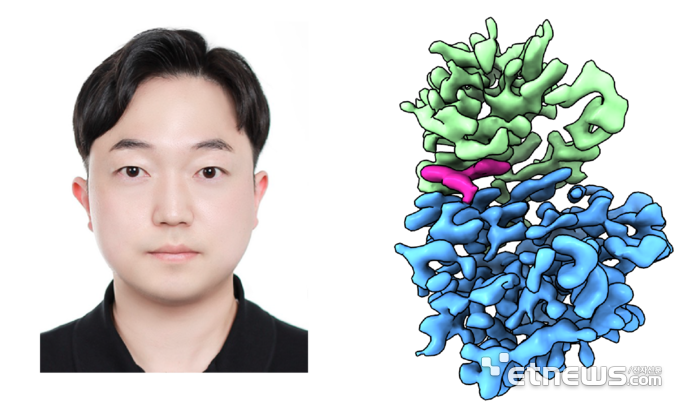
이번 연구에서 연구팀은 초저온전자현미경으로 말토스(당의 한 종류)를 결합한 말토스결합단백질(약 41kDa) 구조를 2.4A(옹스트롬, 10-10미터 또는 0.1nm) 해상도로 규명했다. 나아가 표적항암제인 온반서팁이 결합한 PLK1(약 32 kDa)의 구조를 3.4A 해상도로 규명하는 데 성공했다. 이는 기존 이론적 한계를 뛰어넘는 성과로, 초저온전자현미경을 이용해 소형 단백질의 구조 규명은 물론 약물과의 상호작용 분석까지 가능함을 입증한 것이다.
김동영 교수는 “이번 연구는 현재 상용화된 초저온전자현미경 장비로도 이론적 한계를 넘어서는 소형 단백질의 구조 분석이 가능함을 보여주었다. 나아가 약물의 결합 상태까지 정밀하게 확인할 수 있음을 입증했다는 점에서 초저온전자현미경의 응용 범위를 크게 확장한 데 의의가 있다”면서 “장비 발전과 함께 숙련된 전문 연구 인력의 양성이 중요함을 보여준다”고 밝혔다.
이번 연구는 신약 개발 플랫폼 기업인 바오밥에이바이오(대표 노경태)의 초저온전자현미경 장비를 이용했으며, 이 기업 박건웅 박사(영남대 대학원 약학과 박사 졸업, 제1저자) 주도로 진행됐다. 지난해 7월 바이오아카이브(BioRxiv)에 공개된 이번 연구 논문 초안은 세계적 학술지 사이언스(Science) 공식 블로그에 소개돼 주목받았다. 개정된 논문은 지난달 국제학술지 '네이처 커뮤니케이션즈(Nature Communications)' 온라인판에 게재됐다.
대구=정재훈 기자


 1
1 2
2 3
3 4
4 5
5